
Miễn dịch là gì – Cách tăng miễn dịch đơn giản mà hiệu quả
19/09/2024
Bệnh gút và lời khuyên điều trị
16/12/2024Tổng quan
Chúng tôi đang nghiên cứu chi tiết và làm sáng tỏ cơ chế mà các tế bào miễn dịch nhận diện và tấn công các tế bào ung thư (miễn dịch ung thư). Ngoài ra, chúng tôi cũng đang nghiên cứu phát triển liệu pháp miễn dịch ung thư, trong đó miễn dịch ung thư được điều khiển nhân tạo để áp dụng vào điều trị, và phát triển các loại thuốc tăng cường miễn dịch ung thư.

Trong lĩnh vực nghiên cứu đáp ứng miễn dịch khối u, chúng tôi tập trung vào nghiên cứu miễn dịch ung thư của các tế bào miễn dịch gọi là tế bào sát thủ tự nhiên (NK). Nghiên cứu miễn dịch ung thư và phát triển liệu pháp miễn dịch hiện đang tập trung vào các tế bào miễn dịch gọi là tế bào T. Tuy nhiên, hiệu quả điều trị của các liệu pháp miễn dịch ung thư hiện tại chưa đủ và chỉ giới hạn ở một số loại ung thư có thể chữa khỏi hoàn toàn. Do đó, cần phát triển các liệu pháp miễn dịch mới nhằm tăng cường chức năng của các tế bào miễn dịch liên quan đến miễn dịch ung thư ngoài tế bào T. Tế bào NK có đặc tính tấn công và loại bỏ các tế bào ung thư mà tế bào T không thể loại bỏ, do đó được coi là hữu ích cho việc phát triển liệu pháp miễn dịch thế hệ tiếp theo. Tuy nhiên, hiện tại chưa có phương pháp điều trị nào được thiết lập để tăng cường miễn dịch ung thư của tế bào NK. Chúng tôi mong muốn đóng góp vào việc tiêu diệt ung thư thông qua nghiên cứu về tế bào NK. Để đạt được điều này, trước tiên chúng tôi tiến hành nghiên cứu cơ bản để hiểu sâu hơn về tế bào NK bằng cách làm sáng tỏ các hiện tượng từ khi tế bào NK gặp tế bào ung thư, nhận diện chúng là mục tiêu cần loại bỏ, kích hoạt để tấn công, thể hiện hoạt tính gây độc tế bào, thay đổi tính chất (phân hóa), và cuối cùng là chết tế bào. Trên cơ sở đó, chúng tôi sử dụng những hiểu biết thu được từ nghiên cứu cơ bản để tìm kiếm các loại thuốc tăng cường miễn dịch ung thư của tế bào NK, nghiên cứu phát triển liệu pháp miễn dịch ung thư sử dụng tế bào NK biến đổi gen, và nghiên cứu chuyển giao nhằm phát triển liệu pháp miễn dịch có thể chữa khỏi ung thư bằng cách sử dụng tế bào NK.
Những gì chúng tôi hướng tới
Chúng tôi hướng tới phát triển liệu pháp miễn dịch có thể chữa khỏi ung thư bằng cách sử dụng tế bào NK. Để đạt được mục tiêu này, chúng tôi dựa trên nghiên cứu cơ bản để hiểu rõ bản chất của miễn dịch ung thư do tế bào NK gây ra ở mức độ phân tử, và từ đó xây dựng các nghiên cứu chuyển giao nhằm tăng cường miễn dịch ung thư của tế bào NK một cách nhân tạo.
Địa chỉ liên lạc
- Lĩnh vực nghiên cứu đáp ứng miễn dịch khối u - Trưởng lĩnh vực: Tsukasa Nabekura
- Địa chỉ: 1-1 Kanokoden, Chikusa-ku, Nagoya 464-8681
- Điện thoại: 052-762-6111 (nội bộ 7020)
- Email: [email protected]
Nội dung nghiên cứu Dành cho công chúng
Tổng quan hoạt động nghiên cứu
Trong cơ thể chúng ta, có các tế bào miễn dịch như tế bào NK và tế bào T có khả năng loại bỏ ung thư. Bằng cách làm sáng tỏ cơ chế mà các tế bào miễn dịch này nhận diện, kích hoạt và tiêu diệt các tế bào ung thư (miễn dịch ung thư), chúng tôi hướng tới việc tăng cường miễn dịch ung thư để phát triển các phương pháp điều trị và thuốc hiệu quả hơn. Trong lĩnh vực nghiên cứu đáp ứng miễn dịch khối u, chúng tôi tập trung vào nghiên cứu miễn dịch ung thư do tế bào NK gây ra. Hiện nay, nghiên cứu phát triển liệu pháp miễn dịch chống ung thư chủ yếu tập trung vào tế bào T. Tuy nhiên, hiệu quả điều trị của các liệu pháp miễn dịch ung thư hiện tại chưa đủ và chỉ giới hạn ở một số loại ung thư có thể chữa khỏi hoàn toàn. Ngoài ra, các liệu pháp miễn dịch hiện tại đôi khi gây ra các tác dụng phụ nghiêm trọng. Do đó, cần thiết phải phát triển các liệu pháp miễn dịch mới an toàn hơn và hiệu quả hơn. Tế bào NK có đặc tính tấn công và loại bỏ các tế bào ung thư mà tế bào T không thể loại bỏ, do đó được coi là hữu ích cho việc phát triển liệu pháp miễn dịch thế hệ tiếp theo. Tuy nhiên, cho đến nay, chưa có thuốc hay phương pháp điều trị nào được thiết lập để tăng cường chức năng của tế bào NK. Chúng tôi đặt mục tiêu cuối cùng là đóng góp vào việc tiêu diệt ung thư thông qua nghiên cứu về tế bào NK. Do đó, trước tiên chúng tôi tiến hành nghiên cứu cơ bản để hiểu rõ hơn về cơ chế nhận diện và tấn công tế bào ung thư của tế bào NK ở mức độ phân tử. Trên cơ sở đó, chúng tôi sử dụng những hiểu biết thu được từ nghiên cứu cơ bản để tìm kiếm các loại thuốc tăng cường miễn dịch ung thư của tế bào NK, nghiên cứu phát triển liệu pháp miễn dịch ung thư sử dụng tế bào NK, và nghiên cứu chuyển giao. Sau đó, thông qua các thử nghiệm lâm sàng, chúng tôi xác nhận tính an toàn và hiệu quả của các phương pháp điều trị mới, với mục tiêu cuối cùng là cung cấp liệu pháp điều trị ung thư bằng tế bào NK.
Chủ đề nghiên cứu
(1) Tế bào NK là gì?
Trong cơ thể chúng ta, có các tế bào miễn dịch như tế bào NK và tế bào T có khả năng loại bỏ ung thư. Tế bào T nhận diện các mảnh protein ung thư được trình diện bởi kháng nguyên bạch cầu người (HLA) trên bề mặt tế bào ung thư thông qua một loại protein gọi là thụ thể tế bào T. Sau đó, tế bào T được kích hoạt và tấn công tế bào ung thư (Hình 1). Tuy nhiên, tế bào ung thư có thể giảm hoặc mất biểu hiện HLA khi trở nên ác tính, khiến tế bào T khó nhận diện và cuối cùng thoát khỏi sự tấn công của tế bào T. Thực tế, 25-75% bệnh nhân ung thư cho thấy sự giảm hoặc mất biểu hiện HLA trên tế bào ung thư.
Ngược lại, tế bào NK có thể nhận diện và kích hoạt để tấn công các tế bào ung thư có biểu hiện HLA giảm mà tế bào T không thể nhận diện, thông qua nhiều loại thụ thể NK khác nhau (Hình 1). Như vậy, tế bào NK và tế bào T đóng vai trò bổ sung cho nhau trong miễn dịch ung thư. Do đó, nếu tăng cường miễn dịch ung thư của tế bào NK, có thể điều trị được các loại ung thư mà liệu pháp miễn dịch bằng tế bào T không thể chữa khỏi, khiến tế bào NK trở thành một phương pháp điều trị ung thư tiềm năng. Tuy nhiên, cho đến nay, chưa có thuốc hay liệu pháp nào được phát triển để tăng cường miễn dịch ung thư của tế bào NK.
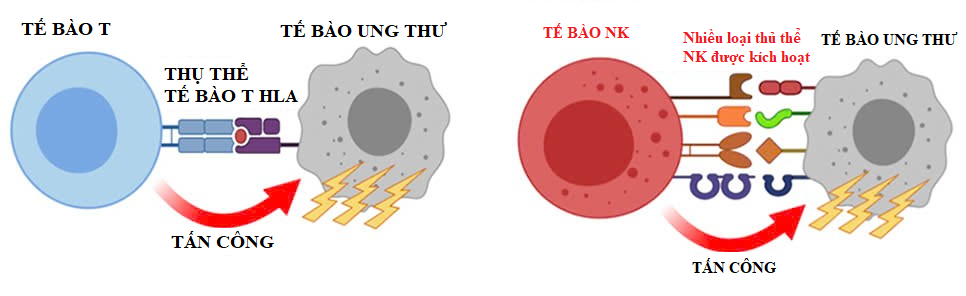
Hình 1. Miễn dịch ung thư của tế bào T và tế bào NK
Tế bào T nhận diện các mảnh protein ung thư được trình diện bởi HLA trên bề mặt tế bào ung thư thông qua thụ thể tế bào T. Tuy nhiên, nhiều tế bào ung thư ở bệnh nhân có thể giảm hoặc mất biểu hiện HLA, khiến tế bào T khó nhận diện và thoát khỏi miễn dịch ung thư của tế bào T. Tế bào NK có thể nhận diện và tấn công các tế bào ung thư có biểu hiện HLA giảm thông qua nhiều loại thụ thể NK khác nhau. Do đó, nếu tăng cường miễn dịch ung thư của tế bào NK, có thể dẫn đến các phương pháp điều trị ung thư hiệu quả hơn.
Chúng tôi đang tiến hành nghiên cứu cơ bản để làm sáng tỏ các hiện tượng từ khi tế bào NK nhận diện, kích hoạt và tấn công tế bào ung thư ở mức độ phân tử. Hơn nữa, chúng tôi sử dụng những hiểu biết từ nghiên cứu cơ bản để phát triển các loại thuốc và liệu pháp miễn dịch sử dụng tế bào NK biến đổi gen nhằm tăng cường khả năng nhận diện và tấn công tế bào ung thư của tế bào NK.
(2) Nội dung nghiên cứu trong lĩnh vực này
Tế bào NK cùng với tế bào T đảm nhận vai trò kép trong miễn dịch ung thư. Do đó, phương pháp điều trị tăng cường miễn dịch ung thư của tế bào NK có thể mang lại hiệu quả điều trị cộng hưởng khi kết hợp với các phương pháp tăng cường miễn dịch ung thư của tế bào T truyền thống. Chúng tôi tiếp cận rộng rãi từ nghiên cứu cơ bản đến nghiên cứu chuyển giao để tăng cường miễn dịch ung thư của tế bào NK.
- 1. Xác định thụ thể NK, ligand và điểm kiểm soát miễn dịch, và nghiên cứu phát triển thuốc nhắm vào các mục tiêu này
Tế bào NK nhận diện tế bào ung thư thông qua việc biểu hiện nhiều loại thụ thể NK khác nhau. Mỗi thụ thể NK liên kết với các protein (ligand) khác nhau trên bề mặt tế bào ung thư (Hình 2). Thụ thể NK bao gồm thụ thể kích hoạt NK truyền tín hiệu kích hoạt tế bào NK và thụ thể ức chế NK truyền tín hiệu ức chế hoạt động của tế bào NK. Thụ thể kích hoạt NK liên kết với các ligand biểu hiện nhiều trên bề mặt tế bào ung thư, kích hoạt tế bào NK (vai trò của bàn đạp ga). Ngược lại, nhiều thụ thể ức chế NK liên kết với HLA, ức chế hoạt động và tấn công của tế bào NK (vai trò của phanh).
Tế bào bình thường không biểu hiện ligand của thụ thể kích hoạt NK và biểu hiện HLA là ligand của thụ thể ức chế NK, do đó tế bào NK không nhận tín hiệu kích hoạt từ thụ thể kích hoạt NK và không tấn công tế bào bình thường (bàn đạp ga < phanh). Ngược lại, tế bào ung thư biểu hiện nhiều ligand của thụ thể kích hoạt NK và giảm biểu hiện HLA để tránh tế bào T. Do đó, khi tế bào NK gặp tế bào ung thư, nó nhận tín hiệu từ thụ thể kích hoạt NK nhưng không nhận tín hiệu từ thụ thể ức chế NK, dẫn đến tế bào NK được kích hoạt và tấn công tế bào ung thư (bàn đạp ga > phanh).
Như vậy, tế bào NK tấn công tế bào ung thư dựa trên sự cân bằng tín hiệu nhận được từ thụ thể kích hoạt và thụ thể ức chế (cân bằng giữa bàn đạp ga và phanh), và tấn công tế bào ung thư theo cường độ tín hiệu từ thụ thể kích hoạt (Hình 2). Tuy nhiên, không phải tất cả các ligand của thụ thể NK đều đã được xác định. Cũng có những thụ thể NK chưa được xác định nhận diện các ligand biểu hiện nhiều trên tế bào ung thư. Chúng tôi đang xác định và phân tích chức năng của các thụ thể NK và ligand chưa biết này để làm sáng tỏ vai trò của chúng trong miễn dịch ung thư, và sử dụng chúng để tăng cường kích hoạt tế bào NK một cách nhân tạo nhằm ứng dụng lâm sàng.
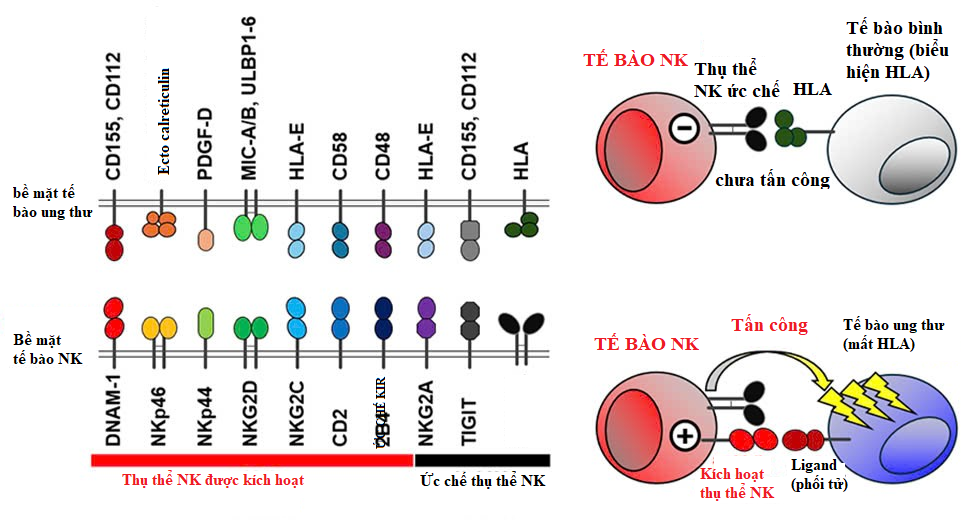
Hình 2. Cơ chế nhận diện và tấn công ung thư của tế bào NK
(Trái) Tế bào NK biểu hiện nhiều loại thụ thể NK khác nhau. Thụ thể kích hoạt NK liên kết với các ligand trên bề mặt tế bào ung thư và truyền tín hiệu kích hoạt đến tế bào NK (vai trò của bàn đạp ga). Ngược lại, nhiều thụ thể ức chế NK liên kết với HLA và truyền tín hiệu ức chế hoạt động của tế bào NK (vai trò của phanh).
(Phải) Tế bào bình thường biểu hiện HLA nhưng không biểu hiện ligand của thụ thể kích hoạt NK. Do đó, khi tế bào NK gặp tế bào bình thường, nó không nhận tín hiệu từ thụ thể kích hoạt NK và không tấn công (bàn đạp ga < phanh). Ngược lại, tế bào ung thư giảm biểu hiện HLA và đồng thời biểu hiện nhiều ligand của thụ thể kích hoạt NK. Do đó, khi tế bào NK gặp tế bào ung thư, nó nhận tín hiệu từ thụ thể kích hoạt NK nhưng không nhận tín hiệu từ thụ thể ức chế NK, dẫn đến tế bào NK được kích hoạt và tấn công tế bào ung thư (bàn đạp ga > phanh).
Ngoài ra, do có ít báo cáo về các thụ thể và phân tử ức chế hoạt động của tế bào NK, chúng tôi đặc biệt chú trọng đến các phân tử ức chế miễn dịch ung thư của tế bào NK. Các chất ức chế điểm kiểm soát miễn dịch gần đây được chú ý là các chế phẩm tăng cường miễn dịch ung thư của tế bào T. Chúng tăng cường khả năng tấn công của tế bào T nhận diện ung thư bằng cách ngăn chặn chức năng của các phân tử điểm kiểm soát miễn dịch ức chế tế bào T. Tuy nhiên, tế bào NK hầu như không biểu hiện các phân tử điểm kiểm soát miễn dịch đã được phát hiện. Do đó, một phương pháp tăng cường miễn dịch ung thư của tế bào NK là phát hiện các phân tử điểm kiểm soát miễn dịch mới của tế bào NK và phát triển các thuốc ngăn chặn chức năng của chúng. Hiện tại, chúng tôi đang xác định và phân tích chức năng của các phân tử điểm kiểm soát miễn dịch của tế bào NK. Nếu có thể ngăn chặn chức năng của các phân tử này bằng cách biến đổi gen hoặc sử dụng thuốc, tế bào NK có thể tấn công tế bào ung thư mạnh mẽ hơn. Chúng tôi đang nghiên cứu cơ chế phân tử ức chế miễn dịch ung thư của tế bào NK và đồng thời tìm kiếm các hợp chất và thuốc đã được phê duyệt để tăng cường miễn dịch ung thư của tế bào NK.
- 2. Nghiên cứu biệt hóa tế bào nhớ của tế bào NK
Đặc điểm lớn nhất của hệ miễn dịch là trí nhớ miễn dịch. Trí nhớ miễn dịch là hiện tượng khi cơ thể tái nhiễm một mầm bệnh đã từng nhiễm trước đó, sẽ kích hoạt phản ứng miễn dịch nhanh hơn và mạnh hơn, duy trì khả năng bảo vệ ưu việt đối với mầm bệnh đó trong thời gian dài. Vắc-xin chống lại các bệnh truyền nhiễm là ứng dụng của trí nhớ miễn dịch trong y học. Trí nhớ miễn dịch được đảm nhận bởi tế bào T thông qua quá trình phân hóa thành tế bào T nhớ (sự thay đổi tính chất không thể đảo ngược). Tế bào T nhớ là những tế bào sống lâu, tồn tại trong cơ thể từ vài năm đến suốt đời, và khi gặp lại mầm bệnh hoặc tế bào ung thư đã từng gặp, chúng có khả năng tấn công mạnh mẽ hơn.
Gần đây, người ta đã phát hiện rằng trí nhớ miễn dịch hiệu quả và bền vững đối với ung thư phụ thuộc vào tế bào T nhớ nhận diện ung thư. Trong khi đó, tuổi thọ của tế bào NK trong cơ thể chỉ từ 1-2 tuần và chúng chết sau khi tấn công tế bào ung thư. Do đó, từ khi được phát hiện, người ta tin rằng tế bào NK không phân hóa thành tế bào sống lâu như tế bào T nhớ và không tham gia vào trí nhớ miễn dịch.
Tuy nhiên, gần đây đã có phát hiện đảo ngược định kiến này: sau khi nhiễm virus, tế bào NK có thể phân hóa thành tế bào NK nhớ với khả năng tấn công mạnh mẽ và đóng góp vào việc bảo vệ chống lại nhiễm virus trong thời gian dài nhờ tín hiệu từ thụ thể kích hoạt NK. Tế bào NK nhớ, khác với tế bào NK thông thường, có tuổi thọ dài, có thể tái sinh và tấn công hiệu quả các tế bào nhiễm virus (Hình 3). Chúng tôi đã phát hiện rằng tế bào NK nhớ có thể tấn công mạnh mẽ tế bào ung thư (Hình 3). Do đó, tế bào NK nhớ được coi là hữu ích cho việc phát triển liệu pháp miễn dịch tế bào mới chống ung thư.
Tuy nhiên, cơ chế phân hóa thành tế bào NK nhớ và duy trì chức năng ưu việt của chúng chưa được làm sáng tỏ đầy đủ. Ngoài ra, không giống như nhiễm virus, ở bệnh nhân ung thư không quan sát thấy sự phân hóa của tế bào NK thành tế bào NK nhớ, cho thấy có thể thiếu một số điều kiện cần thiết để tế bào NK phân hóa thành tế bào NK nhớ trong ung thư.
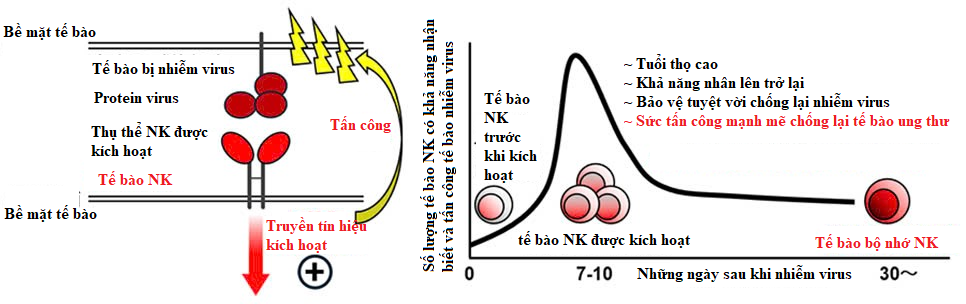
Hình 3. Sự phân hóa tế bào NK thành tế bào NK nhớ
(Trái) Tế bào NK biểu hiện thụ thể kích hoạt NK nhận diện protein virus trên bề mặt tế bào nhiễm virus và nhận tín hiệu kích hoạt từ thụ thể kích hoạt NK, sau đó tấn công tế bào nhiễm virus.
(Phải) Sau khi được kích hoạt bởi nhiễm virus, tế bào NK phân hóa thành tế bào NK nhớ có tuổi thọ dài và khả năng tấn công mạnh mẽ. Tế bào NK nhớ có thể tái sinh và tấn công hiệu quả các tế bào nhiễm virus. Ngoài ra, tế bào NK nhớ còn có khả năng tấn công mạnh mẽ tế bào ung thư.
Chúng tôi hướng tới việc ứng dụng các chức năng ưu việt của tế bào NK nhớ sau nhiễm virus vào điều trị ung thư. Bước đầu tiên là nghiên cứu cơ bản để làm sáng tỏ cơ chế phân hóa và chức năng của tế bào NK nhớ ở mức độ phân tử. Hơn nữa, chúng tôi đang phát triển phương pháp nhân tạo để phân hóa tế bào NK thành tế bào NK nhớ và sử dụng khả năng miễn dịch mạnh mẽ của tế bào NK nhớ để phát triển liệu pháp miễn dịch ung thư thế hệ tiếp theo.。
- 3. Phát triển liệu pháp miễn dịch tế bào NK mới
Gần đây, liệu pháp miễn dịch tế bào ung thư sử dụng các tế bào miễn dịch được biến đổi gen làm thuốc điều trị đã thu hút sự chú ý. Trong đó, liệu pháp CAR-T sử dụng tế bào T của bệnh nhân ung thư được biến đổi gen để biểu hiện thụ thể nhân tạo (Chimeric Antigen Receptor - CAR) có khả năng nhận diện ung thư và truyền vào cơ thể bệnh nhân, đã cho thấy hiệu quả cao đối với một số bệnh ung thư máu khó chữa (như bạch cầu và u lympho). CAR liên kết với các protein biểu hiện nhiều trên tế bào ung thư và truyền tín hiệu kích hoạt mạnh mẽ đến tế bào T, giúp tế bào T tấn công mạnh mẽ tế bào ung thư. Tuy nhiên, liệu pháp CAR-T đôi khi gây ra các tác dụng phụ nghiêm trọng. Ngoài ra, CAR-T cần được điều chỉnh riêng từ tế bào T trong máu của bệnh nhân, do đó, đối với các loại ung thư tiến triển nhanh, thời gian điều chỉnh CAR-T có thể kéo dài và không kịp điều trị, hoặc có nguy cơ thất bại trong quá trình điều chỉnh.
Để khắc phục những vấn đề này, liệu pháp CAR-NK đã được chú ý. Kết quả thử nghiệm lâm sàng mới nhất của liệu pháp CAR-NK cho thấy hiệu quả đối với các khối u máu mà không gây ra tác dụng phụ nghiêm trọng, chứng tỏ liệu pháp CAR-NK có độ an toàn cao. CAR-NK có thể được điều chỉnh từ máu hoặc máu cuống rốn của người khỏe mạnh, sau đó tăng sinh và lưu trữ để sẵn sàng điều trị cho nhiều bệnh nhân ung thư. Tuy nhiên, CAR-NK hiện tại có tuổi thọ ngắn trong cơ thể bệnh nhân và không tăng sinh khi gặp tế bào ung thư, do đó hiệu quả điều trị đối với các khối u máu khó chữa chưa đủ cao
Chúng tôi đang nỗ lực khắc phục những nhược điểm này của liệu pháp CAR-NK bằng cách phát triển CAR-NK cải tiến có thể sống lâu trong cơ thể, nhận diện và tăng sinh khi gặp tế bào ung thư, tấn công mạnh mẽ và loại bỏ tế bào ung thư, đồng thời đảm bảo an toàn và hiệu quả (Hình 4). Ngoài ra, chúng tôi cũng đang cải tiến CAR hiện tại để phù hợp với tế bào NK, phát triển CAR-NK có thể sử dụng cho nhiều loại ung thư khác nhau, và nghiên cứu các vật liệu, phương pháp tăng sinh hiệu quả và lưu trữ thích hợp cho CAR-NK, nhằm xây dựng nền tảng kỹ thuật cho liệu pháp tế bào NK thế hệ tiếp theo (Hình 4).
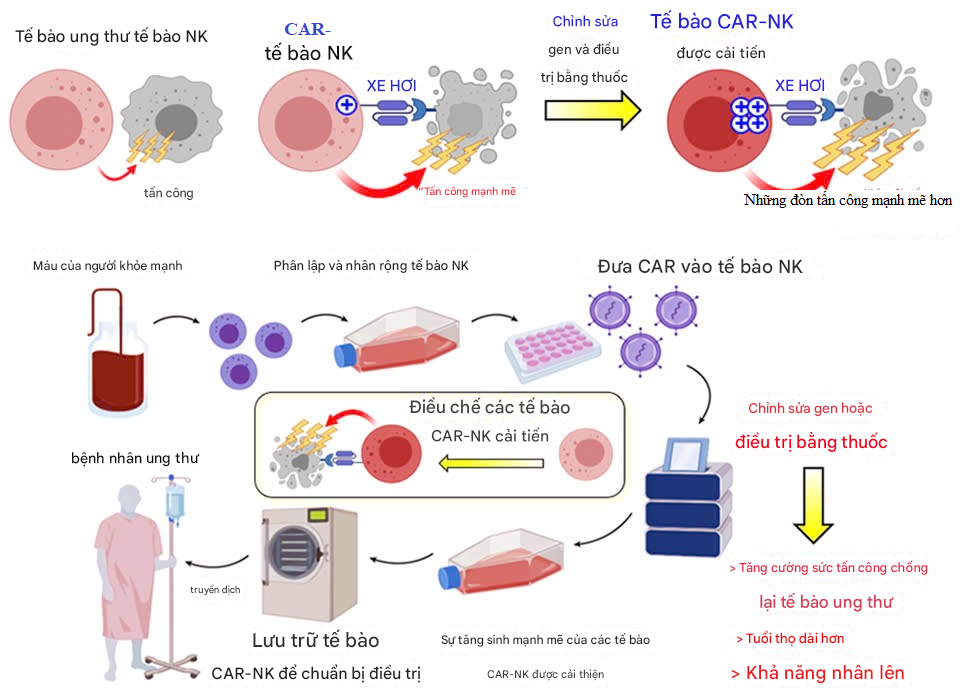
Hình 4. Phát triển kỹ thuật liệu pháp CAR-NK thế hệ tiếp theo
(Trên) Tế bào CAR-NK nhận diện tế bào ung thư thông qua CAR và nhận tín hiệu kích hoạt từ CAR, thể hiện khả năng tấn công mạnh mẽ đối với tế bào ung thư. Bằng cách tăng cường chức năng của tế bào CAR-NK thông qua biến đổi gen hoặc xử lý bằng thuốc, chúng tôi phát triển tế bào CAR-NK cải tiến với khả năng tấn công mạnh mẽ hơn.
(Dưới) Sau khi tách và tăng sinh tế bào NK từ máu của người khỏe mạnh, chúng tôi đưa CAR vào tế bào NK để điều chỉnh thành tế bào CAR-NK. Sau đó, bằng cách biến đổi gen hoặc xử lý bằng thuốc, chúng tôi tăng cường khả năng tấn công, kéo dài tuổi thọ và khả năng tăng sinh của tế bào CAR-NK. Cuối cùng, chúng tôi tăng sinh tế bào CAR-NK với số lượng lớn và lưu trữ để sẵn sàng điều trị cho bệnh nhân ung thư.
Những gì chúng tôi hướng tới
Hiện tại, chưa có thuốc điều trị nào có thể tăng cường miễn dịch ung thư bằng tế bào NK một cách nhân tạo, cũng như liệu pháp miễn dịch sử dụng tế bào NK để chữa khỏi ung thư. Cơ chế nhận diện ung thư của tế bào NK thông qua các thụ thể NK khác nhau, tích hợp tín hiệu kích hoạt trong tế bào và điều chỉnh sức mạnh tấn công ung thư vẫn chưa được hiểu rõ hoàn toàn. Chúng tôi mong muốn phát triển các loại thuốc tăng cường miễn dịch ung thư bằng tế bào NK và liệu pháp miễn dịch tế bào NK thế hệ tiếp theo thông qua việc hiểu sâu hơn về tế bào NK.
Nội dung nghiên cứu dành cho chuyên gia
Tầm nhìn - Bức tranh lớn - Mục tiêu
- Tầm nhìn của chúng tôi là xóa bỏ hoàn toàn ung thư.
- Bức tranh lớn của chúng tôi là hiểu rõ tế bào NK và làm sáng tỏ bản chất của miễn dịch ung thư bằng tế bào NK.
- Mục tiêu của chúng tôi là đóng góp cho xã hội thông qua việc phát triển liệu pháp miễn dịch có thể chữa khỏi ung thư dựa trên sinh học tế bào NK.
Để đạt được mục tiêu này, chúng tôi sẽ kết hợp chặt chẽ các lĩnh vực nghiên cứu cơ bản, nghiên cứu chuyển giao và nghiên cứu lâm sàng, dựa trên nền tảng miễn dịch học và sinh học tế bào. Chúng tôi sẽ tích hợp các kiến thức và kỹ thuật từ nhiều lĩnh vực như sinh học, y học và kỹ thuật để phát triển nghiên cứu độc đáo của mình nhằm điều trị ung thư.
Bối cảnh nghiên cứu
| Tế bào NK là gì?
Tế bào NK chỉ chiếm khoảng 2-10% tế bào lympho trong máu ngoại vi. Tuy nhiên, tế bào NK đóng vai trò thiết yếu trong việc kiểm soát ung thư. Ngoài ra, tế bào NK cũng cần thiết để kiểm soát các bệnh nhiễm virus thuộc họ herpes như cytomegalovirus (CMV), và tham gia vào việc kiểm soát các bệnh nhiễm virus có thể gây tử vong như viêm gan, Ebola, HIV, SARS-CoV-2. Tế bào NK nhận diện và kích hoạt khi gặp các tế bào ung thư hoặc tế bào bất thường, giải phóng các hạt gây độc tế bào chứa perforin và granzyme để tiêu diệt các tế bào mục tiêu. Đồng thời, tế bào NK kích hoạt cũng sản xuất các cytokine và chemokine như interferon-gamma (IFN-γ). Hoạt động gây độc tế bào và sản xuất cytokine được gọi là chức năng hiệu ứng.
| Đáp ứng miễn dịch ung thư
Tế bào NK và tế bào T CD8+ là các tế bào miễn dịch đảm nhận vai trò miễn dịch ung thư. Tế bào T CD8+ nhận diện peptide từ kháng nguyên ung thư được trình diện bởi phân tử phức hợp hòa hợp mô chính (MHC) lớp I trên bề mặt tế bào ung thư thông qua một loại thụ thể tế bào T duy nhất. Sau đó, tế bào T CD8+ được kích hoạt và thể hiện hoạt động gây độc tế bào đối với tế bào ung thư (Hình 1). Tuy nhiên, tế bào ung thư giảm hoặc mất biểu hiện phân tử MHC lớp I để tránh đáp ứng miễn dịch của tế bào T CD8+ trong quá trình ác tính hóa. Khoảng 25-75% bệnh nhân ung thư có sự giảm hoặc mất biểu hiện MHC lớp I trên tế bào ung thư. Trong khi đó, tế bào NK nhận diện và kích hoạt thông qua các thụ thể NK đa dạng khi gặp tế bào ung thư giảm biểu hiện MHC lớp I mà tế bào T CD8+ không thể nhận diện, thể hiện hoạt động gây độc tế bào (Hình 1). Như vậy, tế bào NK và tế bào T đóng vai trò bổ sung cho nhau và đều cần thiết trong miễn dịch ung thư. Hình 1. Cơ chế nhận diện tế bào ung thư của tế bào T và tế bào NK
Tế bào T nhận diện peptide từ kháng nguyên ung thư được trình diện bởi phân tử MHC lớp I thông qua một loại thụ thể tế bào T duy nhất. Tuy nhiên, trong 25-75% bệnh nhân ung thư, tế bào ung thư giảm hoặc mất biểu hiện MHC lớp I, giúp chúng tránh được miễn dịch của tế bào T. Tế bào NK nhận diện và kích hoạt thông qua các thụ thể NK đa dạng khi gặp tế bào ung thư giảm biểu hiện MHC lớp I, thể hiện hoạt động gây độc tế bào. Như vậy, tế bào NK và tế bào T đóng vai trò bổ sung cho nhau và đều cần thiết trong miễn dịch ung thư.
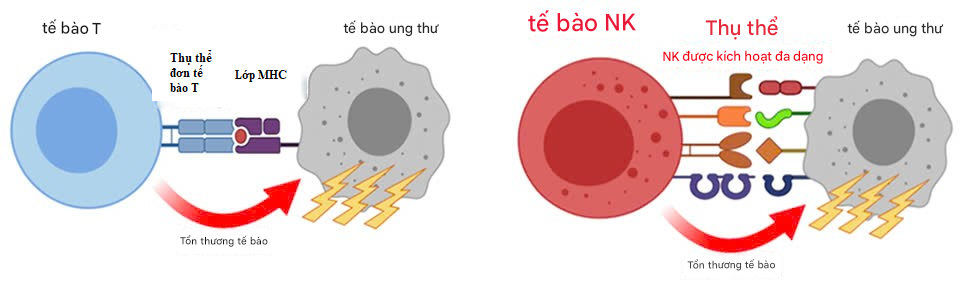
Hình 1. Cơ chế nhận diện tế bào ung thư của tế bào T và tế bào NK
Tế bào T nhận diện peptide từ kháng nguyên ung thư được trình diện bởi phân tử MHC lớp I thông qua một loại thụ thể tế bào T duy nhất. Tuy nhiên, trong 25-75% bệnh nhân ung thư, tế bào ung thư giảm hoặc mất biểu hiện MHC lớp I, giúp chúng tránh được miễn dịch của tế bào T. Tế bào NK nhận diện và kích hoạt thông qua các thụ thể NK đa dạng khi gặp tế bào ung thư giảm biểu hiện MHC lớp I, thể hiện hoạt động gây độc tế bào. Như vậy, tế bào NK và tế bào T đóng vai trò bổ sung cho nhau và đều cần thiết trong miễn dịch ung thư.
| Thách thức của liệu pháp miễn dịch ung thư
Liệu pháp miễn dịch, tiêu biểu là các chất ức chế điểm kiểm soát miễn dịch, đã khẳng định vị trí như một lựa chọn điều trị ung thư. Tuy nhiên, hiệu quả điều trị của liệu pháp miễn dịch ung thư vẫn còn hạn chế và chỉ có một số loại ung thư có thể được chữa khỏi hoàn toàn. Ngoài ra, liệu pháp miễn dịch ung thư hiện tại đôi khi gây ra các tác dụng phụ nghiêm trọng. Do đó, luôn cần phát triển các liệu pháp miễn dịch mới có độ an toàn và hiệu quả cao, với cơ chế tác động khác biệt, nhằm khắc phục sự kháng thuốc của ung thư đối với các phương pháp điều trị hiện có và tạo ra hiệu quả điều trị cộng hưởng khi kết hợp với các phương pháp truyền thống.
Nghiên cứu phát triển liệu pháp miễn dịch ung thư chủ yếu tập trung vào tế bào T. Một trong những cơ chế kháng điều trị chính của liệu pháp miễn dịch ung thư bằng tế bào T là sự giảm biểu hiện của phân tử MHC lớp I trên tế bào ung thư. Tế bào NK có khả năng nhận diện và loại bỏ các tế bào ung thư giảm biểu hiện MHC lớp I mà tế bào T không thể nhận diện. Vì tế bào NK và tế bào T đều đóng vai trò quan trọng trong miễn dịch ung thư, việc kích hoạt đáp ứng miễn dịch ung thư của tế bào NK có thể giúp điều trị các loại ung thư mà liệu pháp miễn dịch bằng tế bào T không thể chữa khỏi. Mặc dù tế bào NK được kỳ vọng sẽ trở thành yếu tố thay đổi cuộc chơi trong điều trị ung thư trong tương lai gần, nhưng hiện tại vẫn chưa có phương pháp điều trị hoặc thuốc nào có thể tăng cường hoạt động chống ung thư của tế bào NK.
Tổng quan nghiên cứu
Trong lĩnh vực nghiên cứu đáp ứng miễn dịch khối u, chúng tôi nghiên cứu đáp ứng miễn dịch ung thư của tế bào NK. Tế bào NK có khả năng nhận diện và loại bỏ các tế bào ung thư mà tế bào T không thể loại bỏ, do đó được coi là hữu ích cho việc phát triển liệu pháp miễn dịch thế hệ tiếp theo. Tuy nhiên, mặc dù có nhiều nỗ lực từ các nhà nghiên cứu trong lĩnh vực này, vẫn chưa có thuốc tăng cường đáp ứng miễn dịch ung thư của tế bào NK hay liệu pháp miễn dịch tế bào NK có thể chữa khỏi ung thư khó chữa. Để thiết lập các phương pháp kích hoạt miễn dịch ung thư của tế bào NK, cần phải hiểu rõ cơ chế phân tử từ việc nhận diện tế bào ung thư bằng thụ thể NK, truyền tín hiệu kích hoạt, đến điều chỉnh chức năng tế bào và thể hiện hoạt động gây độc tế bào. Ngoài ra, việc xác định và phân tích chức năng của các phân tử ức chế mới và các điểm kiểm soát miễn dịch là cần thiết để tăng cường hoạt động chống ung thư của tế bào NK. Chúng tôi hướng tới việc chuyển hóa các kết quả nghiên cứu cơ bản này thành nghiên cứu chuyển giao, phát triển thuốc tăng cường miễn dịch ung thư của tế bào NK và xây dựng nền tảng nghiên cứu và proof-of-concept cho liệu pháp miễn dịch tế bào NK thế hệ tiếp theo. Liệu pháp miễn dịch tế bào NK mới phát triển sẽ được kiểm tra an toàn và hiệu quả trong các thử nghiệm lâm sàng, cuối cùng được cung cấp như một lựa chọn điều trị ung thư.
Nội dung nghiên cứu
Hiện tại, chưa có phương pháp kích hoạt miễn dịch ung thư bằng tế bào NK. Vì tế bào NK và tế bào T đều đóng vai trò quan trọng trong miễn dịch ung thư, các phương pháp điều trị và thuốc tăng cường miễn dịch ung thư của tế bào NK có thể tạo ra hiệu quả điều trị cộng hưởng khi kết hợp với các chất ức chế điểm kiểm soát miễn dịch và thuốc nhắm mục tiêu phân tử hiện có. Chúng tôi tiếp cận nghiên cứu từ cơ bản đến chuyển giao và phát triển thuốc, dựa trên nền tảng miễn dịch học và sinh học tế bào, nhằm kích hoạt đáp ứng miễn dịch ung thư của tế bào NK.
-1. Xác định và phân tích chức năng của thụ thể NK, ligand và điểm kiểm soát miễn dịch, và phát triển thuốc nhắm mục tiêu chúng
Tế bào NK biểu hiện nhiều thụ thể NK kích hoạt và ức chế trên bề mặt tế bào (Hình 2). Thụ thể NK kích hoạt nhận diện các phân tử tăng biểu hiện trên bề mặt tế bào ung thư và truyền tín hiệu kích hoạt, dẫn đến kích hoạt tế bào NK và chức năng hiệu ứng. Ngược lại, nhiều thụ thể NK ức chế nhận diện phân tử MHC lớp I và truyền tín hiệu ức chế đến tế bào NK (Hình 2). Tế bào bình thường biểu hiện MHC lớp I, trong khi nhiều tế bào ung thư giảm biểu hiện MHC lớp I để tránh miễn dịch của tế bào T. Tế bào NK không kích hoạt và không gây độc tế bào bình thường do nhận tín hiệu ức chế từ tương tác thụ thể NK ức chế - MHC lớp I (tín hiệu thụ thể NK kích hoạt < tín hiệu thụ thể NK ức chế) (Hình 2). Ngược lại, tế bào ung thư giảm biểu hiện MHC lớp I, do đó tế bào NK không nhận tín hiệu ức chế từ tương tác với tế bào ung thư. Hơn nữa, tế bào ung thư tăng biểu hiện ligand của thụ thể NK kích hoạt, dẫn đến kích hoạt tế bào NK và gây độc tế bào ung thư (tín hiệu thụ thể NK kích hoạt > tín hiệu thụ thể NK ức chế) (Hình 2). Ngay cả khi tế bào ung thư, tế bào bị tổn thương DNA hoặc tế bào chuyển dạng vẫn biểu hiện MHC lớp I, nếu ligand của thụ thể NK kích hoạt tăng biểu hiện đáng kể, tế bào NK vẫn nhận tín hiệu kích hoạt và gây độc tế bào (tín hiệu thụ thể NK kích hoạt > tín hiệu thụ thể NK ức chế) (Hình 2). Do đó, sự kích hoạt và chức năng hiệu ứng của tế bào NK, cũng như cường độ của chúng, được xác định bởi sự cân bằng và tổng hợp của tín hiệu thụ thể NK kích hoạt và ức chế. Nếu tổng hợp tín hiệu thụ thể NK kích hoạt vượt qua tín hiệu thụ thể NK ức chế, tế bào NK sẽ kích hoạt và thể hiện chức năng hiệu ứng (Hình 2). Kết quả là, tế bào NK có thể chọn lọc gây độc và loại bỏ tế bào ung thư (Hình 2). Vì vậy, việc xác định và phân tích chức năng của thụ thể NK, ligand và các phân tử truyền tín hiệu hạ lưu của thụ thể là chủ đề quan trọng nhất trong sinh học tế bào NK.
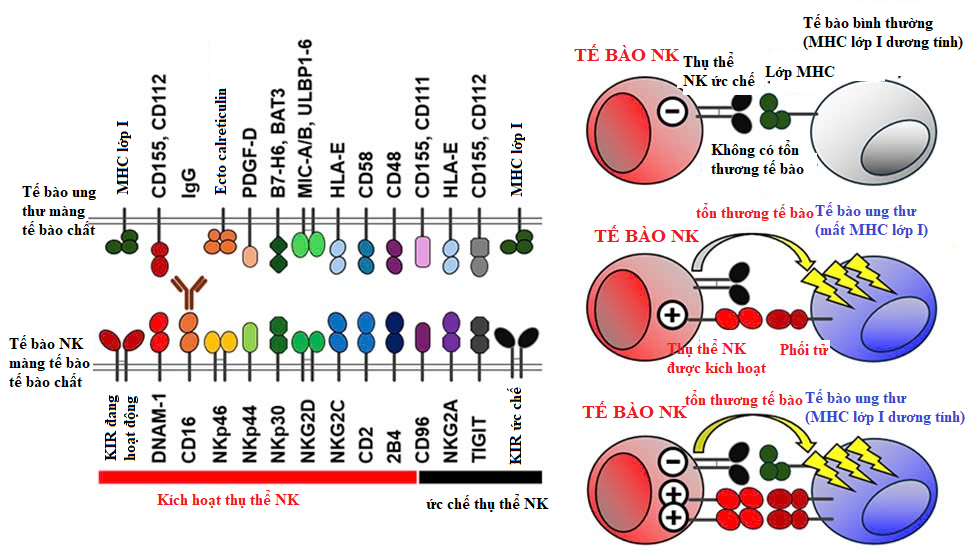
Hình 2. Cơ chế nhận diện tế bào ung thư và nguyên lý hoạt động gây độc tế bào của tế bào NK
(Trái) Tế bào NK biểu hiện nhiều loại thụ thể NK khác nhau. Thụ thể NK kích hoạt nhận diện các ligand do tế bào ung thư biểu hiện. Ngược lại, nhiều thụ thể NK ức chế nhận diện phân tử MHC lớp I.
(Phải) Tế bào bình thường biểu hiện MHC lớp I nhưng không biểu hiện ligand của thụ thể NK kích hoạt. Do đó, tế bào NK không thể hiện hoạt động gây độc tế bào. Ngược lại, tế bào ung thư giảm biểu hiện MHC lớp I và tăng biểu hiện ligand của thụ thể NK kích hoạt. Do đó, tế bào NK nhận tín hiệu từ thụ thể NK kích hoạt và thể hiện hoạt động gây độc tế bào. Ngay cả khi tế bào ung thư vẫn biểu hiện MHC lớp I, nếu ligand của thụ thể NK kích hoạt tăng biểu hiện đáng kể, tín hiệu từ thụ thể NK kích hoạt sẽ vượt qua tín hiệu từ thụ thể NK ức chế, dẫn đến hoạt động gây độc tế bào của tế bào NK. Như vậy, sự kích hoạt và hoạt động gây độc tế bào của tế bào NK, cũng như cường độ của chúng, được quyết định bởi sự cân bằng và tổng hợp của tín hiệu từ thụ thể NK kích hoạt và thụ thể NK ức chế.
Tuy nhiên, không phải tất cả các tương tác thụ thể NK - ligand đều đã được xác định, và một số ligand của thụ thể NK liên quan đến đáp ứng miễn dịch ung thư vẫn chưa được xác định. Việc xác định các thụ thể NK kích hoạt và ức chế nhận diện các phân tử do tế bào ung thư biểu hiện có ý nghĩa quan trọng vì nó có thể dẫn đến việc điều chỉnh miễn dịch ung thư của tế bào NK một cách nhân tạo. Khi nhận diện tế bào ung thư, tế bào NK nhận tín hiệu từ nhiều thụ thể NK kích hoạt và ức chế cùng lúc. Tuy nhiên, cách các tín hiệu này được tích hợp và điều chỉnh trong tế bào vẫn chưa được hiểu rõ hoàn toàn. Chúng tôi mong muốn xác định và phân tích chức năng của các thụ thể NK và ligand chưa biết, cũng như các phân tử liên quan đến cơ chế tích hợp tín hiệu của thụ thể NK, để xác định vai trò của chúng trong miễn dịch ung thư và phát triển các phương pháp tăng cường kích hoạt tế bào NK một cách nhân tạo, ứng dụng vào lâm sàng.
Ngoài ra, các báo cáo về các phân tử ức chế miễn dịch ung thư của tế bào NK còn hạn chế. Một phương pháp tăng cường miễn dịch ung thư của tế bào NK là phát triển các chất ức chế điểm kiểm soát miễn dịch mà tế bào NK biểu hiện hoặc phá hủy gen của các điểm kiểm soát miễn dịch này thông qua biến đổi gen. Tuy nhiên, vì tế bào NK không biểu hiện cao các điểm kiểm soát miễn dịch đã biết, việc xác định và phân tích chức năng của các phân tử ức chế mới và các điểm kiểm soát miễn dịch là cần thiết để tăng cường miễn dịch ung thư của tế bào NK. Các phân tử truyền tín hiệu ức chế các đường truyền tín hiệu của thụ thể NK kích hoạt được coi là mục tiêu tiềm năng cho việc phát triển thuốc tăng cường hoạt động chống ung thư của tế bào NK, nhưng hiện tại các phân tử này chưa được xác định. Gần đây, chúng tôi tập trung vào các phân tử ức chế miễn dịch ung thư của tế bào NK và thực hiện xác định và phân tích chức năng của các điểm kiểm soát miễn dịch của tế bào NK. Hiện tại, chúng tôi đang tiến hành phân tích chức năng chi tiết và làm sáng tỏ cơ chế của các phân tử ức chế mà chúng tôi mới xác định được trong miễn dịch ung thư của tế bào NK. Đồng thời, chúng tôi đang tìm kiếm các hợp chất phân tử nhỏ tăng cường đáp ứng miễn dịch ung thư của tế bào NK và các thuốc đã được phê duyệt có thể tái định vị, thông qua các phương pháp tiếp cận sinh học cấu trúc và sử dụng trí tuệ nhân tạo để tìm kiếm thư viện hợp chất.
- 2. Làm sáng tỏ cơ chế phân tử của sự phân hóa và chức năng của tế bào NK nhớ
Một trong những chức năng đáng chú ý nhất của hệ miễn dịch là trí nhớ miễn dịch. Trí nhớ miễn dịch là hiện tượng khi cơ thể tiếp xúc lại với một kháng nguyên đã từng gặp, sẽ kích hoạt đáp ứng miễn dịch nhanh hơn và mạnh hơn, duy trì khả năng bảo vệ cơ thể trong thời gian dài, như đã thấy ở vắc-xin. Đáp ứng miễn dịch ung thư hiệu quả và bền vững cũng cần có trí nhớ miễn dịch của tế bào T CD8 dương tính. Trí nhớ miễn dịch trước đây được cho là chỉ do tế bào T và B có khả năng phân hóa thành tế bào nhớ đảm nhiệm. Trong khi đó, tế bào NK được cho là tế bào ngắn hạn, chết sau 1-2 tuần và không có khả năng phân hóa thành tế bào nhớ hay tham gia vào trí nhớ miễn dịch.
Tuy nhiên, gần đây đã có phát hiện đảo ngược quan điểm này. Sau khi nhiễm CMV, tế bào NK của chuột biểu hiện thụ thể NK kích hoạt Ly49H và tế bào NK của người biểu hiện thụ thể NK kích hoạt NKG2C có thể nhận diện tế bào nhiễm CMV, tăng sinh đặc hiệu kháng nguyên và phân hóa thành tế bào NK nhớ, góp phần bảo vệ chống nhiễm trùng lâu dài (Hình 3). Các thụ thể NK kích hoạt này nhận diện đặc hiệu protein CMV hoặc các mảnh của nó trên tế bào nhiễm, kết hợp với phân tử truyền tín hiệu DAP12 và truyền tín hiệu kích hoạt qua Syk và Zap70. Tế bào NK kích hoạt thể hiện hoạt động gây độc tế bào và loại bỏ tế bào nhiễm, đảm nhận bảo vệ trong giai đoạn đầu của nhiễm trùng. Sau đó, các tế bào NK kích hoạt này tăng sinh và tồn tại lâu dài trong cơ thể như tế bào NK nhớ.
Tế bào NK nhớ có các đặc điểm: (1) Tăng sinh và tồn tại lâu dài, (2) Biểu hiện các kháng nguyên bề mặt tế bào, biểu hiện gen toàn diện và hồ sơ epigenetic khác biệt so với tế bào NK chưa cảm ứng và tế bào NK kích hoạt, (3) Thể hiện chức năng hiệu ứng vượt trội so với tế bào NK chưa cảm ứng in vitro, (4) Có khả năng tăng sinh thứ cấp khi nhiễm CMV lần thứ hai, (5) Thể hiện khả năng bảo vệ chống nhiễm CMV vượt trội so với tế bào NK chưa cảm ứng, đáp ứng các tiêu chí của trí nhớ miễn dịch và được định nghĩa là tế bào NK nhớ (Hình 3).
Điều thú vị là tế bào NK nhớ thể hiện chức năng hiệu ứng mạnh hơn so với tế bào NK chưa cảm ứng khi kích thích bởi tất cả các thụ thể NK kích hoạt. Điều này được cho là do sự thay đổi toàn diện trong biểu hiện gen và epigenome khi phân hóa thành tế bào nhớ, dẫn đến ngưỡng truyền tín hiệu của thụ thể NK kích hoạt giảm, cho phép tế bào NK nhớ thể hiện chức năng hiệu ứng mạnh mẽ bất kể loại thụ thể NK kích hoạt. Thực tế, tế bào NK nhớ thể hiện hoạt động gây độc tế bào mạnh mẽ đối với các tín hiệu từ thụ thể NK kích hoạt DNAM-1 và NKG2D, quan trọng trong việc loại bỏ ung thư, do đó thể hiện hoạt động chống ung thư mạnh mẽ. Ngoài ra, tế bào NK nhớ thể hiện hoạt động gây độc tế bào phụ thuộc kháng thể (ADCC) mạnh mẽ qua thụ thể NK kích hoạt CD16. Tế bào NK nhớ tăng sinh thứ cấp sau khi tái nhiễm CMV sau ghép tủy hoặc ghép cơ quan, góp phần kiểm soát nhiễm trùng. Hơn nữa, tế bào NK nhớ có thể ngăn ngừa sự nghiêm trọng của nhiễm HIV và SARS-CoV-2. Ý nghĩa lâm sàng quan trọng của trí nhớ miễn dịch tế bào NK là tế bào NK nhớ loại bỏ các bệnh lý tồn dư nhỏ ở bệnh nhân ung thư huyết học, giảm tỷ lệ tái phát và cải thiện tỷ lệ sống sót của bệnh nhân. Hoạt động ADCC mạnh mẽ của tế bào NK nhớ cũng có thể góp phần vào hiệu quả điều trị của các thuốc kháng thể như Trastuzumab, Cetuximab, Rituximab và Avelumab.
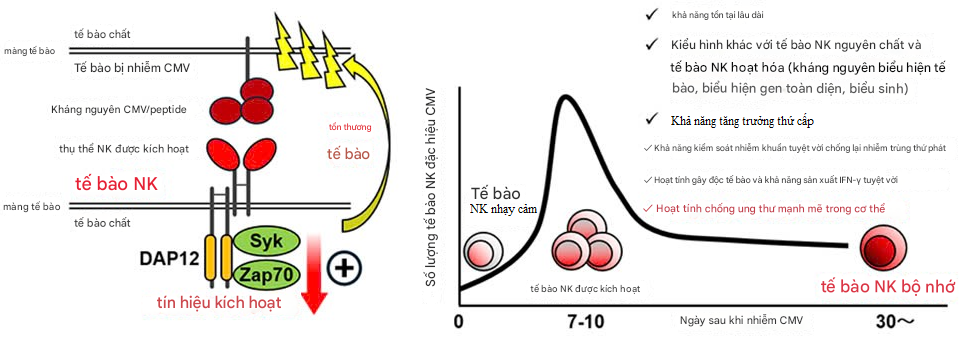
Hình 3. Sự phân hóa của tế bào NK nhớ
(Trái) Tế bào NK của chuột biểu hiện thụ thể NK kích hoạt Ly49H và tế bào NK của người biểu hiện thụ thể NK kích hoạt NKG2C nhận diện đặc hiệu kháng nguyên CMV hoặc peptide của nó trên tế bào nhiễm CMV, và được kích hoạt qua tín hiệu từ thụ thể NK kích hoạt. Ly49H và NKG2C kết hợp với phân tử truyền tín hiệu DAP12 và truyền tín hiệu kích hoạt qua Syk và Zap70. Tế bào NK đặc hiệu CMV đã được kích hoạt thể hiện hoạt động gây độc tế bào đối với tế bào nhiễm.
(Phải) Sau khi nhiễm CMV, tế bào NK đặc hiệu CMV đã được kích hoạt tăng sinh đặc hiệu kháng nguyên và phân hóa thành tế bào NK nhớ tồn tại lâu dài. Tế bào NK nhớ thể hiện kiểu hình khác biệt so với tế bào NK chưa cảm ứng và tế bào NK kích hoạt, có khả năng tăng sinh thứ cấp và bảo vệ chống nhiễm trùng vượt trội khi nhiễm CMV lần thứ hai. Tế bào NK nhớ thể hiện hoạt động gây độc tế bào và khả năng sản xuất IFN-γ mạnh mẽ khi kích thích bởi tất cả các thụ thể NK kích hoạt, và thể hiện hoạt động chống ung thư mạnh mẽ trong cơ thể.
Chúng tôi đã phát hiện rằng tế bào NK nhớ có hoạt động chống ung thư mạnh mẽ khi nghiên cứu trí nhớ miễn dịch của tế bào NK với mục tiêu ứng dụng vào miễn dịch ung thư. Tế bào NK nhớ không chỉ có hoạt động chống ung thư mạnh mẽ mà còn có khả năng tồn tại lâu dài, hoạt động gây độc tế bào và khả năng tăng sinh vượt trội. Những đặc điểm này của tế bào NK nhớ có thể hữu ích trong việc phát triển liệu pháp miễn dịch ung thư, do đó việc làm sáng tỏ cơ chế phân tử của sự phân hóa và chức năng của chúng có ý nghĩa quan trọng về mặt cơ bản và lâm sàng. Cho đến nay, các nhóm nghiên cứu, bao gồm cả chúng tôi, đã xác định vai trò của nhiều phân tử liên quan đến tế bào NK như thụ thể NK, cytokine, phân tử truyền tín hiệu và yếu tố phiên mã. Tuy nhiên, bản chất của trí nhớ miễn dịch tế bào NK vẫn chưa được hiểu rõ và chưa đạt đến mức độ hiểu biết về trí nhớ miễn dịch của tế bào T. Ngoài ra, cho đến nay, sự phân hóa của tế bào NK nhớ chưa được quan sát thấy ở bệnh nhân ung thư, cho thấy rằng các yếu tố môi trường và tín hiệu cần thiết cho sự hình thành trí nhớ miễn dịch tế bào NK có thể thiếu trong ung thư.
Trong tương lai, cần nghiên cứu các bệnh mà sự phân hóa của tế bào NK nhớ được quan sát, các tương tác thụ thể NK - ligand và các đường truyền tín hiệu cytokine thúc đẩy sự phân hóa của tế bào NK nhớ, cũng như xác định và phân tích chức năng của các yếu tố phiên mã và epigenetic quyết định danh tính của tế bào NK nhớ để hiểu rõ hơn về trí nhớ miễn dịch tế bào NK. Chúng tôi đang tiến hành nghiên cứu cơ bản để làm sáng tỏ trí nhớ miễn dịch tế bào NK ở mức độ phân tử. Đồng thời, thông qua việc làm sáng tỏ cơ chế phân tử của trí nhớ miễn dịch tế bào NK, chúng tôi hướng tới việc ứng dụng các đặc tính của tế bào NK nhớ vào miễn dịch ung thư bằng cách tăng cường miễn dịch ung thư của tế bào NK thông qua phân hóa tế bào NK nhớ nhân tạo bằng cách sử dụng gene, chỉnh sửa genome và hợp chất, hoặc tái kích hoạt tế bào NK đã xâm nhập vào khối u và rơi vào trạng thái kiệt sức.
- 3. Xây dựng nền tảng nghiên cứu cho liệu pháp miễn dịch tế bào NK thế hệ tiếp theo
Hiệu quả của liệu pháp miễn dịch chống ung thư vẫn chưa đủ cao và chỉ có một số loại ung thư có thể chữa khỏi hoàn toàn. Một trong những liệu pháp mới được phát triển gần đây là liệu pháp tế bào T thụ thể kháng nguyên chimeric (CAR). Tế bào T được biến đổi gen để biểu hiện thụ thể CAR, có khả năng nhận diện đặc hiệu tế bào ung thư và kích hoạt tín hiệu CAR để thể hiện hoạt động gây độc tế bào. Liệu pháp CAR-T, trong đó tế bào T của bệnh nhân được tách ra, biến đổi gen để biểu hiện CAR và truyền lại vào cơ thể bệnh nhân, đã cho thấy hiệu quả cao đối với các khối u tế bào B khó điều trị. Tuy nhiên, liệu pháp này có thể gây ra các tác dụng phụ nghiêm trọng như hội chứng giải phóng cytokine và độc tính thần kinh. Ngoài ra, CAR-T cần được điều chỉnh riêng lẻ từ tế bào T của bệnh nhân, điều này có thể làm mất cơ hội điều trị cho các bệnh nhân ung thư tiến triển nhanh hoặc có nguy cơ thất bại trong quá trình điều chỉnh.
Để khắc phục những vấn đề này, tế bào NK đã thu hút sự chú ý. Gần đây, liệu pháp CAR-NK đã được phát triển như một phương pháp kích hoạt miễn dịch ung thư của tế bào NK. Các thử nghiệm lâm sàng sử dụng tế bào CAR-NK từ máu cuống rốn của người khác đã báo cáo hiệu quả đối với các khối u tế bào B mà không có các tác dụng phụ nghiêm trọng như hội chứng giải phóng cytokine hoặc độc tính thần kinh, cho thấy liệu pháp CAR-NK an toàn hơn so với CAR-T. Ngoài ra, tế bào CAR-NK từ máu cuống rốn hoặc máu ngoại vi của người khỏe mạnh có thể được điều chỉnh và bảo quản với số lượng lớn, có tiềm năng sử dụng như một sản phẩm "off-the-shelf" trong tương lai. Hơn nữa, tế bào CAR-NK có thể nhận diện tế bào ung thư không chỉ qua CAR mà còn qua các thụ thể NK kích hoạt nội tại, góp phần tăng cường hoạt động gây độc tế bào và loại bỏ tế bào ung thư.
Tuy nhiên, tế bào CAR-NK hiện tại có khả năng sống sót kém trong cơ thể bệnh nhân, khả năng tăng sinh sau khi nhận diện tế bào ung thư thấp và hiệu quả điều trị đối với các khối u tế bào B khó điều trị còn hạn chế. Ngoài ra, hầu hết các CAR được sử dụng để điều chỉnh tế bào CAR-NK đều là thế hệ thứ hai từ liệu pháp CAR-T, trong khi liệu pháp CAR-T đã phát triển đến thế hệ thứ năm, cho thấy cấu trúc CAR chưa được tối ưu hóa cho tế bào NK.
Chúng tôi đang nỗ lực khắc phục những vấn đề này bằng cách cải thiện tế bào CAR-NK thông qua biến đổi gen, chỉnh sửa genome, tối ưu hóa nuôi cấy cytokine và xử lý thuốc để tăng cường khả năng sống sót lâu dài và khả năng tăng sinh, đồng thời tăng cường hoạt động chống ung thư (Hình 4). Chúng tôi cũng đang nghiên cứu tạo ra tế bào CAR-NK ít bị kiệt sức khi xâm nhập vào khối u thông qua biến đổi gen. Đồng thời, việc làm sáng tỏ cơ chế phân tử của sự tăng cường chức năng tế bào và hiệu quả điều trị của tế bào CAR-NK có thể giúp xác định các yếu tố ức chế mới và các phân tử mục tiêu điều trị, mở ra hướng nghiên cứu và phát triển liệu pháp tế bào NK cải tiến với hiệu quả điều trị cao hơn.
Ngoài ra, chúng tôi đang hướng tới việc thiết lập các phương pháp nuôi cấy và vật liệu tốt hơn cho việc tăng sinh tế bào NK, phương pháp biến đổi gen và chỉnh sửa genome hiệu quả cao cho tế bào NK, tối ưu hóa cấu trúc CAR chuyên biệt cho tế bào NK, phát triển CAR có thể ứng dụng cho nhiều loại ung thư, thiết lập điều kiện nuôi cấy để tăng sinh tế bào CAR-NK với hoạt động chống ung thư cao, nghiên cứu phương pháp bảo quản tối ưu và xây dựng ngân hàng tế bào, và phát triển chương trình lựa chọn lô tế bào CAR-NK an toàn và hiệu quả tối đa dựa trên hồ sơ MLA, KIR và nhiễm CMV của bệnh nhân ung thư và người hiến tặng (Hình 4). Thông qua các nghiên cứu và phát triển này, chúng tôi sẽ xây dựng nền tảng nghiên cứu cho liệu pháp tế bào NK thế hệ tiếp theo.
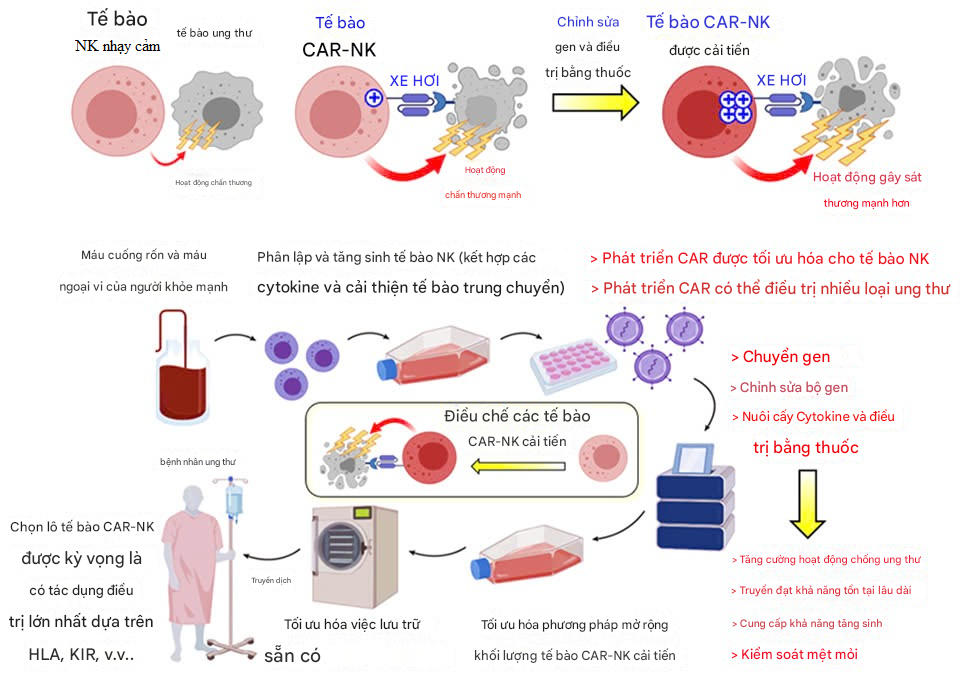
Hình 4. Xây dựng nền tảng nghiên cứu và phát triển liệu pháp CAR-NK thế hệ tiếp theo
(Trên) Tế bào CAR-NK nhận diện tế bào ung thư qua CAR, kích hoạt tín hiệu CAR và thể hiện hoạt động gây độc mạnh mẽ. Bằng cách tăng cường chức năng của tế bào CAR-NK thông qua biến đổi gen và xử lý thuốc, chúng tôi phát triển các tế bào CAR-NK cải tiến với hoạt động gây độc mạnh hơn.
(Dưới) Tế bào NK được tách từ máu cuống rốn của người khác hoặc máu ngoại vi của người khỏe mạnh, sau đó được nuôi cấy trong điều kiện tối ưu và biến đổi gen để biểu hiện CAR. Chúng tôi phát triển các CAR tối ưu hóa cho tế bào NK và có thể ứng dụng cho nhiều loại ung thư. Ngoài ra, chúng tôi kích hoạt các chức năng tế bào khác nhau thông qua biến đổi gen, chỉnh sửa genome, nuôi cấy cytokine tối ưu và xử lý thuốc. Chúng tôi cũng điều chỉnh tế bào CAR-NK với số lượng lớn, tối ưu hóa phương pháp bảo quản và xây dựng ngân hàng tế bào để sử dụng như sản phẩm "off-the-shelf". Chúng tôi lựa chọn lô tế bào CAR-NK cải tiến an toàn và hiệu quả tối đa dựa trên HLA, KIR của bệnh nhân và các yếu tố khác, sau đó truyền vào cơ thể bệnh nhân.
Giới thiệu nhân viên
Tsukasa Nabekura
Chức vụ: Trưởng lĩnh vực
Tiểu sử:
Sinh ra tại Nanae, Hokkaido. Tốt nghiệp Đại học Tsukuba năm 2003, nhận bằng Tiến sĩ Y khoa năm 2008. Từ năm 2008 đến 2011, nghiên cứu viên tại Phòng thí nghiệm Miễn dịch học, Đại học Tsukuba. Từ năm 2011 đến 2016, nghiên cứu viên tại Khoa Vi sinh và Miễn dịch học, Đại học California, San Francisco. Từ năm 2014 đến 2018, trợ lý giáo sư tại Trung tâm Nghiên cứu Liên ngành về Khoa học Sự sống, Đại học Tsukuba. Từ năm 2018 đến 2024, trợ lý giáo sư tại Trung tâm Nghiên cứu Động lực học Sự sống, Đại học Tsukuba. Đảm nhận vị trí hiện tại từ tháng 6 năm 2024.

Chủ đề nghiên cứu chính:
- Làm sáng tỏ cơ chế nhận diện tế bào đích và tích hợp tín hiệu của thụ thể NK.
- Làm sáng tỏ cơ chế phân tử trong hình thành trí nhớ miễn dịch của tế bào NK.
- Xây dựng nền tảng nghiên cứu cho liệu pháp miễn dịch tế bào NK thế hệ tiếp theo, bao gồm liệu pháp CAR-NK.
- Phát triển và tái định vị thuốc nhắm mục tiêu phân tử để kích hoạt đáp ứng miễn dịch của tế bào NK chống ung thư.
- Xác định và phân tích chức năng của các yếu tố điều hòa quy định sự phát triển và hoạt động gây độc tế bào của tế bào NK.
- Xác định và phân tích chức năng của các thụ thể NK mới, ligand NK, phân tử điểm kiểm soát miễn dịch, phân tử truyền tín hiệu, yếu tố phiên mã và yếu tố epigenetic điều khiển đáp ứng miễn dịch của tế bào NK.
- Làm sáng tỏ cơ chế kiệt sức của tế bào NK trong miễn dịch chống ung thư.
Thông điệp
Tế bào NK kiểm soát ung thư bằng cách tiêu diệt tế bào ung thư mà không làm hại tế bào bình thường. Do đó, ý nghĩa tồn tại của chúng rất đơn giản và rõ ràng. Tuy nhiên, sự phát triển, hoạt động gây độc tế bào, cơ chế nhận diện tế bào bất thường và sự phân hóa của tế bào NK vẫn còn nhiều điều chưa biết, và cơ chế phân tử từ khi nhận diện mục tiêu đến khi thể hiện hoạt động gây độc tế bào rất phức tạp và khó hiểu. Tuy nhiên, chắc chắn có lý do sinh học phức tạp và khó hiểu đằng sau điều này, và việc tiếp cận nó là cốt lõi của nghiên cứu tế bào NK. Hiểu rõ sự phức tạp của tế bào NK sẽ giúp chúng ta hiểu rõ hơn về tế bào NK và miễn dịch tế bào NK chống ung thư, từ đó phát triển liệu pháp miễn dịch ung thư thế hệ tiếp theo sử dụng tế bào NK. Chúng tôi tìm kiếm những người quan tâm đến nghiên cứu tế bào NK, có nhiệt huyết tham gia nghiên cứu cơ bản về tế bào NK và có tư duy cầu nối nghiên cứu ứng dụng lâm sàng miễn dịch tế bào NK chống ung thư.
- Hirokazu Tajima - Chức vụ: Kỹ thuật viên
- Mizuho Enomoto - Chức vụ: Kỹ thuật viên nghiên cứu
- Atsuko Mizuno - Chức vụ: Thư ký
Nguồn tham khảo: https://cancer-c.pref.aichi.jp/research-institute/immune-response/
Dịch: CÔNG TY TNHH SHIOKAZE


