Quang Miễn Dịch – hy vọng của bệnh nhân ung thư
30/10/2020
Top 3 cách bổ sung chất xơ hiệu quả (phần 2)
03/11/2020Phê duyệt thuốc Akalux – Nguồn tiếng Nhật (Báo Nikkei Nhật Bản): https://www.nikkei.com/article/DGXMZO64278330V20C20A9EA5000/?s=5
Nguồn tiếng Trung (Báo The Paper): https://bom.to/klN7kK4
Người dịch: Ngọc Quỳnh, kiểm tra và hiệu chỉnh: Hoàng Triều.
Hoàn thành ngày 23/10/2020
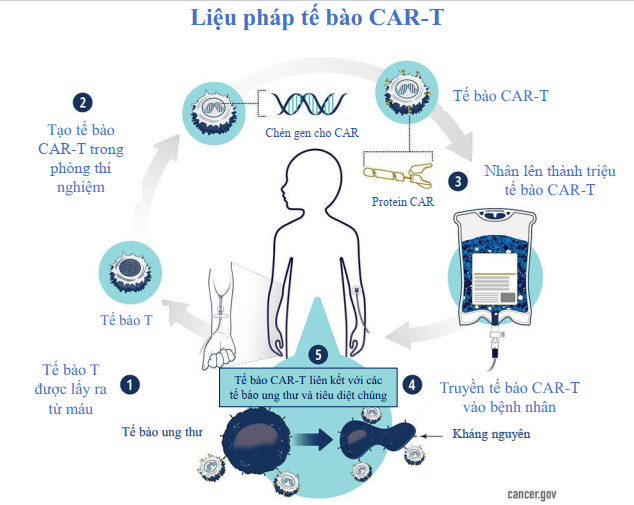
Quang Miễn Dịch là phương pháp điều trị ung thư thứ năm trên Thế giới
Rakuten Medical (California, Mỹ) thuộc Tập đoàn Rakuten vào ngày 25/09/2020 thông báo đã nhận được sự chấp thuận của Bộ Y tế, Lao động và Phúc lợi Nhật Bản về việc sản xuất và buôn bán loại thuốc mới được sử dụng trong điều trị ung thư có tên là “Quang Miễn Dịch”. Liệu pháp này đang thu hút sự chú ý với tư cách là “phương pháp điều trị ung thư thứ 5” sau phẫu thuật, xạ trị, hóa trị và thuốc tăng miễn dịch trị ung thư. Phương pháp này giúp điều trị các loại Ung thư vùng Đầu và Cổ, là các loại Ung thư vốn rất khó điều trị bằng các phương pháp trước đây.
Thuốc được phê duyệt tên là “Cetuximab Sarotalocan Sodium” (tên sản phẩm là Akalux) được sử dụng trong liệu pháp Quang Miễn Dịch. Nó có đặc tính là có thể bám vào các protein trên bề mặt tế bào ung thư.
Khi được rọi ánh sáng lazer, nó sẽ gây ra phản ứng hóa học và giúp tiêu diệt chính xác các tế bào ung thư. Bộ Y tế, Lao động và Phúc lợi Nhật bản đã phê duyệt cho phép điều trị các trường hợp ung thư tái phát hoặc ung thư vùng đầu và cổ mà không thể điều trị bằng phẫu thuật.

Tiến trình đưa phương pháp Quang Miễn Dịch đến với bệnh nhân ung thư
Công ty con của Rakuten Medical Nhật Bản đã nộp đơn xin phê duyệt vào tháng 3 năm nay (2020). Vào năm 2019, Bộ Y tế, Lao động và Phúc lợi Nhật đã chỉ định loại thuốc Akalux cho liệu pháp này là đối tượng để áp dụng hệ thống kiểm đinh tốc độ cao, để từ đó phê duyệt loại thuốc này ở Nhật Bản trước khi ra thế giới.
Ngoài ra, mặc dù thông thường phải thử nghiệm lâm sàng qua ba giai đoạn (thử nghiệm lâm sàng). Tuy nhiên trong năm nay, một chế độ đặc biệt được áp dụng để thông qua mà không cần đợi kết quả thử nghiệm cuối cùng lâm sàng giai đoạn 3. Dự kiến cuối năm 2020 Nhật sẽ quyết định giá thuốc và áp dụng bảo hiểm y tế công cho thuốc này ở khung điều trị bệnh hiểm nghèo, ít có thuốc đặc dụng.
Mặt khác, công ty cần báo cáo số liệu chi tiết về hiệu quả và tính an toàn ngay cả sau khi thuốc được bán ra. Nếu không đáp ứng các điều kiện này có thể dẫn đến việc thu hồi phê duyệt loại thuốc này. Quang Miễn Dịch là một liệu pháp được phát triển bởi ông Hisataka Kobayashi, người nghiên cứu ung thư tại Viện Y tế Công cộng Quốc gia (NIH) ở Hoa Kỳ và bắt đầu thử nghiệm lâm sàng tại Hoa Kỳ từ năm 2015. Trong thử nghiệm giai đoạn 2 tại Hoa Kỳ, hơn 40% bệnh nhân đã xác nhận tế bào ung thư được thu nhỏ hoặc được loại bỏ.
Hệ thống laser được sử dụng cho liệu pháp này cũng đã được Bộ Y tế, Lao động và Phúc lợi xã hội cho phép sản xuất và bán vào ngày 2 tháng 9. Trong tương lai, Rakuten Medical sẽ hợp tác với các cơ sở y tế trong và ngoài nước để đẩy mạnh nghiên cứu các ứng dụng khác ngoài điều trị ung thư vùng đầu và cổ.
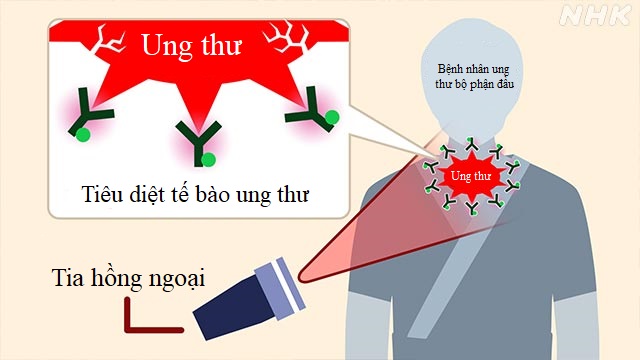
Thông tin thêm từ báo “The Paper” Trung Quốc:
Thuốc Akalux chứa các kháng thể tấn công tế bào ung thư và các hóa chất có thể phản ứng với ánh sáng. Thuốc được dùng cho bệnh nhân qua đường tiêm. Sau khi thuốc và tế bào ung thư dính vào nhau, bệnh nhân được chiếu tia laser cận hồng ngoại để kích hoạt các kháng thể trong thuốc sau đó tiêu diệt đúng tế bào ung thư. Phương pháp điều trị như vậy được gọi là liệu pháp Quang Miễn Dịch.
Trong các thử nghiệm lâm sàng được thực hiện tại Nhật Bản và Hoa Kỳ, tính an toàn và hiệu quả nhất định của Akalux đã được các bác sĩ và chuyên viên nghiên cứu khẳng định.
Theo tờ “Mainichi Shimbun” (Báo Hằng ngày – Nhật bản), trong quá trình thử nghiệm lâm sàng loại thuốc này tại Hoa Kỳ, mặc dù bệnh nhân có các triệu chứng như đau và sưng, nhưng không xuất hiện tác dụng phụ nghiêm trọng do thuốc Akalux gây ra.
Tham khảo các bài viết về Quang Miễn Dịch và thuốc Akalux:
Quang Miễn Dịch – hy vọng của bệnh nhân ung thư
Phương pháp điều trị ung thư mới nhất “Quang Miễn Dịch”